简介
自然杀伤细胞,也称为NK 细胞或大颗粒淋巴细胞( LGL ),是一种对先天免疫系统至关重要的细胞毒性 淋巴细胞。它们属于快速扩增的已知先天淋巴细胞(ILC)家族,占人类所有循环淋巴细胞的 5-20%。 NK 细胞的作用类似于脊椎动物适应性免疫反应中的细胞毒性 T 细胞。NK 细胞基于来自几种激活和抑制受体的信号,对病毒感染细胞、应激细胞、肿瘤细胞和其他细胞内病原体做出快速反应。大多数免疫细胞检测受感染细胞表面的主要组织相容性复合体 I (MHC-I)上呈递的抗原,但 NK 细胞可以在没有抗体和 MHC 的情况下识别和杀死应激细胞,从而实现更快的免疫反应。它们被称为“自然杀伤细胞”,因为它们不需要激活就可以杀死缺少MHC I 类“自身”标记的细胞。这一作用尤为重要,因为缺少 MHC I 标记的有害细胞无法被其他免疫细胞(如 T 淋巴细胞)检测和摧毁。
NK 细胞可通过CD56的存在和CD3的缺失(CD56 +、 CD3 −)来识别。NK 细胞由CD127 +共同先天淋巴祖细胞分化而来,后者位于共同淋巴祖细胞的下游, B淋巴细胞和T 淋巴细胞也源自于此。已知 NK 细胞在骨髓、淋巴结、脾脏、扁桃体和胸腺中分化和成熟,然后进入血液循环。NK 细胞在表型上与自然杀伤 T 细胞(NKT)不同,其来源和各自的效应功能不同;通常,NKT 细胞活性通过分泌干扰素 γ来促进 NK 细胞活性。与 NKT 细胞不同,NK 细胞不表达T 细胞抗原受体(TCR) 或泛 T 细胞标记CD3或表面免疫球蛋白(Ig) B 细胞受体,但它们通常在人类中表达表面标记CD16 (FcγRIII) 和CD57 ,在C57BL/6 小鼠中表达NK1.1或 NK1.2。NKp46细胞表面标记目前是另一种首选 NK 细胞标记,在人类、几种小鼠品系(包括BALB/c 小鼠)和三种常见猴类中均有表达。
在先天免疫之外,激活和抑制NK细胞受体在自我耐受和维持NK细胞活性中都发挥着重要的功能作用。NK细胞在适应性免疫反应中也发挥作用:大量实验表明,NK细胞能够迅速适应周围环境并形成抗原特异性免疫记忆,这对于应对相同抗原的继发感染至关重要。在使用 NK 细胞活性作为潜在癌症治疗和 HIV 治疗 的研究中,NK 细胞在先天和适应性免疫反应中的作用变得越来越重要。
人类自然杀伤细胞,彩色扫描电子显微照片
早期历史
在早期针对癌症患者和动物模型的细胞介导细胞毒性实验中,研究人员不断观察到所谓的“自然”反应;也就是说,某些细胞群似乎能够摧毁肿瘤细胞,而无需事先对它们产生敏感性。利兹大学医学院的亨利·史密斯博士于 1966 年首次发表了一项研究,声称未经处理的淋巴样细胞能够赋予对肿瘤的天然免疫力,得出的结论是“这种现象似乎是正常小鼠对肿瘤生长的防御机制的表现”。其他研究人员也做出了类似的观察,但由于这些发现与当时建立的模型不一致,许多人最初认为这些观察结果是人为的。
到 1973 年,多种物种中都发现了“自然杀伤”活性,并推测存在具有这种能力的独立细胞谱系。20 世纪 70 年代初,博士生 Rolf Kiessling 和博士后研究员 Hugh Pross 在小鼠中以及 Hugh Pross 和博士生 Mikael Jondal 在人类中发现了一种独特类型的淋巴细胞是“自然”或自发细胞毒性的原因。小鼠和人类的研究分别在斯德哥尔摩卡罗琳斯卡医学院的Eva Klein和 Hans Wigzell 教授的指导下进行。Kiessling 的研究涉及 T 淋巴细胞攻击先前已免疫的肿瘤细胞的明确能力。Pross 和 Jondal 正在研究正常人体血液中的细胞介导细胞毒性以及去除各种带有受体的细胞对这种细胞毒性的影响。同年晚些时候,罗纳德·赫伯曼 (Ronald Herberman)发表了关于小鼠效应细胞独特性质的类似数据。人类数据大部分由 West等人使用类似技术和相同的红白血病靶细胞系K562证实。K562 对人类 NK 细胞裂解高度敏感,几十年来,K562 51铬释放试验已成为检测人类 NK 功能活性最常用的试验。 它几乎被广泛使用,这意味着世界各地的不同实验室可以轻松比较实验数据。
利用不连续密度离心法,以及后来的单克隆抗体,人们将自然杀伤能力定位到如今被称为 NK 细胞的大型颗粒淋巴细胞亚群上。1980 年,Timonen 和 Saksela 证明密度梯度分离的大颗粒淋巴细胞负责人类 NK 活性,这是 NK 细胞首次在显微镜下可视化,是该领域的一项重大突破。
类型
NK 细胞可分为 CD56 bright或 CD56 dim。CD56 bright NK细胞与T 辅助细胞类似,通过释放细胞因子发挥作用。CD56 bright NK 细胞占 NK细胞的大多数,存在于骨髓、次级淋巴组织、肝脏和皮肤中。CD56 bright NK 细胞的特点是优先杀死高度增殖的细胞,因此可能具有免疫调节作用。CD56 dimNK 细胞主要存在于外周血中,以其细胞杀伤能力为特征。CD56 dimNK 细胞始终为CD16阳性(CD16 是抗体依赖性细胞毒作用(ADCC)的关键介质)。CD56 bright可以通过获得 CD16转变为 CD56 dim
NK 细胞可通过 CD16 介导的 ADCC 消除病毒感染的细胞。所有2019 冠状病毒病(COVID-19) 患者的 CD56 bright NK 细胞均已耗竭,但 CD56 dim仅在重症 COVID-19 患者中耗竭。
受体
NK 细胞受体也可根据功能进行区分。天然细胞毒性受体在与直接指示细胞感染的Fas 配体结合后直接诱导细胞凋亡(细胞死亡) 。MHC 非依赖性受体(如上所述)使用替代途径诱导受感染细胞凋亡。自然杀伤细胞活化由抑制和激活受体刺激的平衡决定。例如,如果抑制受体信号更突出,则 NK 细胞活性将受到抑制;同样,如果激活信号占主导地位,则会导致 NK 细胞活化。
NK 细胞受体类型(具有抑制性以及一些激活性成员)根据结构进行区分,以下是一些例子:
激活受体
Ly49 (同型二聚体)是一种相对较古老的 C 型凝集素家族受体,在小鼠中存在多基因,而人类仅具有一种假基因Ly49,即经典(多态性) MHC I分子的受体。
NCR(天然细胞毒性受体)是免疫球蛋白超家族的 1 型跨膜蛋白,在刺激后介导 NK 杀伤和IFNγ的释放。它们与病毒配体(如血凝素和血凝素神经氨酸酶)、一些细菌配体和与肿瘤生长相关的细胞配体(如PCNA)结合。
CD16(FcγIIIA)在抗体依赖性细胞介导的细胞毒作用中发挥作用;特别是,它们与免疫球蛋白G结合。
TLR - Toll 样受体属于模式识别受体 (PRR)组,是先天免疫细胞的典型,但也在 NK 细胞上表达。它们识别PAMP(病原体相关分子模式)和DAMP(损伤相关分子模式)作为配体。这些受体对于诱导免疫反应至关重要。TLR 诱导通过促进炎性细胞因子和趋化因子的产生来放大免疫反应,并最终导致 NK 细胞效应功能的激活。因此,NK 细胞直接对周围环境中的病原体做出反应。除TLR-10外,NK 细胞表达所有人类 TLR,尽管水平不同。NK 细胞表达高水平的TLR-1,中等水平的TLR-2、 TLR-3、 TLR-5和TLR-6,低水平的TLR-4、 TLR-8和 TLR-9 以及极低水平的TLR-7。TLR 受体的表达与它们的激活状态无关,它们与细胞因子和趋化因子协同激活自然杀伤细胞。 这些受体在细胞外表面或内体内表达。除 TLR-3 和 TLR-4 外,所有 TLR 都通过衔接蛋白MyD88发出信号,最终主要导致NF-κB的激活。 TLR-3 通过衔接蛋白TRIF发出信号,而 TLR-4 可以分别在通过 MyD88 和 TRIF 发出信号之间切换。 不同 TLR 的诱导会导致 NK 细胞功能的不同激活。
抑制性受体
杀伤细胞免疫球蛋白样受体(KIR) 属于最近进化的免疫球蛋白样胞外域受体多基因家族;它们存在于非人类灵长类动物中,是灵长类动物经典 MHC I(HLA-A、HLA-B、HLA-C)和非经典 Mamu-G(HLA-G)的主要受体。一些 KIR 特定于某些 HLA 亚型。大多数 KIR 是抑制性和显性的。常规细胞表达 MHC 1 类,因此可被 KIR 受体识别,从而抑制 NK 细胞杀伤。
CD94/NKG2(异二聚体)是一种 C 型凝集素家族受体,在啮齿类动物和灵长类动物中均有存在,可识别非经典(也是非多态性)MHC I 分子,例如HLA-E。HLA-E 在细胞表面的表达依赖于源自经典 MHC I 类分子信号序列的非聚体肽表位的存在,该表位由信号肽肽酶和蛋白酶体的顺序作用产生。虽然是间接的,但这是一种调查经典(多态性)HLA 分子水平的方法。
ILT或LIR(免疫球蛋白样受体)——是最近发现的 Ig 受体家族成员。
Ly49(同型二聚体)既有激活异构体,也有抑制异构体。它们在群体水平上具有高度多态性;尽管它们在结构上与 KIR 无关,但它们是小鼠中 KIR 的功能同源物,包括表达模式。Ly49 是经典(多态性)MHC I 分子的受体。
功能
细胞溶解颗粒介导的细胞凋亡
NK细胞具有细胞毒性;其细胞质中的小颗粒含有蛋白质,例如穿孔素和称为颗粒酶的蛋白酶。穿孔素在靠近要杀死的细胞时,会在靶细胞的细胞膜上形成孔隙,从而创建一个水通道,颗粒酶和相关分子可以通过该通道进入,从而诱导细胞凋亡或渗透性细胞裂解。细胞凋亡和细胞裂解之间的区别在免疫学中很重要:裂解病毒感染的细胞可能会释放病毒体,而细胞凋亡会导致内部病毒的破坏。NK细胞还会分泌抗菌分子α-防御素,它通过破坏细菌细胞壁的方式直接杀死细菌,方式类似于中性粒细胞。
抗体依赖性细胞介导的细胞毒作用(ADCC)
感染细胞通常会被抗体调理,以便免疫细胞检测。与抗原结合的抗体可被NK 细胞上表达的FcγRIII ( CD16 ) 受体识别,从而导致 NK 细胞活化、细胞溶解颗粒释放和随之而来的细胞凋亡。这是一些单克隆抗体(如利妥昔单抗 (Rituxan)、奥法木单抗 (Azzera)等)的主要杀伤机制。抗体依赖性细胞介导的细胞毒性对肿瘤细胞杀伤的贡献可以通过使用NK-92的特定测试来测量,NK-92 是NantKwest, Inc.授权的 NK 样细胞的永生系:将转染了高亲和力Fc 受体的NK-92 细胞的反应与不表达 Fc 受体的“野生型”NK-92 的反应进行比较。
细胞因子诱导的 NK 和细胞毒性 T 淋巴细胞(CTL)激活
细胞因子在 NK 细胞活化中起着至关重要的作用。由于这些是病毒感染后细胞释放的应激分子,它们可以向 NK 细胞发出信号,告知受影响区域存在病毒病原体。参与 NK 活化的细胞因子包括IL-12、IL-15、IL-18、IL-2和CCL5。NK 细胞在干扰素或巨噬细胞衍生的细胞因子的作用下被激活。它们的作用是控制病毒感染,而适应性免疫反应会产生可以清除感染的抗原特异性细胞毒性 T 细胞。NK 细胞通过分泌IFNγ和TNFα来控制病毒感染。IFNγ 激活巨噬细胞进行吞噬和裂解,而 TNFα 则促进 NK 直接杀死肿瘤细胞。事实证明,缺乏 NK 细胞的患者在疱疹病毒感染的早期阶段极易受到影响。
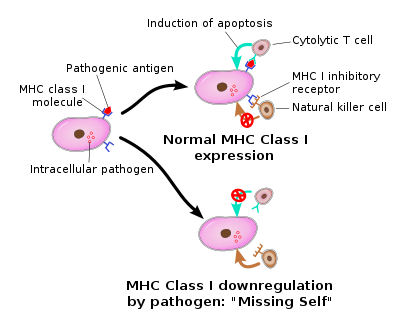
细胞毒性T细胞和NK细胞互补活性示意图
缺失‘自我’假设
NK 细胞要保护身体免受病毒和其他病原体的侵害,就需要能够确定细胞是否被感染的机制。确切的机制仍是当前研究的主题,但人们认为与“改变的自我”状态的识别有关。为了控制其细胞毒性活性,NK 细胞拥有两种类型的表面受体:激活受体和抑制受体,包括杀伤细胞免疫球蛋白样受体。大多数这些受体并非 NK 细胞所独有,也可能存在于某些T 细胞亚群中。
抑制性受体识别MHC I 类 等位基因,这可以解释为什么 NK 细胞优先杀死具有低水平 MHC I 类分子的细胞。这种 NK 细胞靶向相互作用模式被称为“缺失自我识别”,这是Klas Kärre及其同事在 20 世纪 90 年代末创造的一个术语。MHC I 类分子是细胞向细胞毒性 T 细胞展示病毒或肿瘤抗原的主要机制。在细胞内微生物和肿瘤中都可以看到对此的一种常见进化适应:MHC I 分子的慢性下调,使受影响的细胞对 T 细胞不可见,从而使它们能够逃避 T 细胞介导的免疫。NK 细胞显然是对这种适应的进化反应(MHC 的丧失会消除 CD4/CD8 作用,因此另一种免疫细胞进化来履行这一功能)
肿瘤细胞监视
自然杀伤细胞通常缺乏抗原特异性细胞表面受体,因此属于先天免疫的一部分,即能够在未接触病原体的情况下立即作出反应。在小鼠和人类中,即使在没有表面粘附分子和抗原肽的情况下,NK 细胞也可以通过直接诱导肿瘤细胞死亡(NK 细胞充当细胞溶解效应淋巴细胞)在肿瘤免疫监视中发挥作用。NK 细胞的这种作用对于免疫成功至关重要,特别是因为 T 细胞无法在没有表面抗原的情况下识别病原体。肿瘤细胞检测会导致 NK 细胞激活,从而产生和释放细胞因子。
如果肿瘤细胞不引起炎症,它们也会被视为自身,不会诱导 T 细胞反应。NK 细胞会产生许多细胞因子,包括肿瘤坏死因子 α ( TNFα )、IFNγ和白细胞介素( IL-10 )。TNFα 和 IL-10 分别起到促炎和免疫抑制剂的作用。NK 细胞的激活和随后产生的细胞溶解效应细胞会影响巨噬细胞、树突状细胞和中性粒细胞,进而引发抗原特异性 T 细胞和 B 细胞反应。NK 细胞对肿瘤细胞的裂解不是通过抗原特异性受体起作用,而是由其他受体介导的,包括NKG2D、NKp44、NKp46、NKp30 和 DNAM。NKG2D是一种二硫键连接的同型二聚体,可识别许多配体,包括 ULBP 和MICA,这些配体通常在肿瘤细胞上表达。树突状细胞—NK 细胞界面在免疫生物学中的作用已被研究并被定义为对理解复杂的免疫系统至关重要。[需要引用]
NK 细胞以及巨噬细胞和其他几种细胞类型都表达 Fc 受体 (FcR) 分子 (FC-gamma-RIII = CD16),这是一种激活生化受体,可结合IgG 类抗体的Fc部分。这使 NK 细胞能够靶向已发生体液反应的细胞,并通过抗体依赖性细胞毒性 (ADCC)裂解细胞。这种反应取决于 NK 细胞上表达的 Fc 受体的亲和力,NK 细胞对抗体的 Fc 部分具有高、中和低亲和力。这种亲和力由蛋白质 158 位氨基酸决定,可以是苯丙氨酸 (F 等位基因) 或缬氨酸 (V 等位基因)。具有高亲和力 FcRgammRIII (158 V/V 等位基因) 的个体对抗体疗法的反应更好。接受抗体 Rituxan 治疗的淋巴瘤患者已证明这一点。表达 158 V/V 等位基因的患者具有更好的抗肿瘤反应。仅有 15–25% 的人口表达 158 V/V 等位基因。为了确定单克隆抗体的 ADCC 贡献,NK-92 细胞(一种“纯”NK 细胞系)已被转染高亲和力 FcR 基因。
清除衰老细胞
自然杀伤细胞 (NK 细胞) 和巨噬细胞在清除衰老细胞中起主要作用。自然杀伤细胞直接杀死衰老细胞,并产生细胞因子激活巨噬细胞,清除衰老细胞。
自然杀伤细胞可以使用NKG2D受体检测衰老细胞,并使用穿孔素成孔细胞溶解蛋白杀死这些细胞。CD8+ 细胞毒性 T 淋巴细胞也使用 NKG2D 受体检测衰老细胞,并促进类似于 NK 细胞的杀伤作用。例如,在帕金森病患者中,自然杀伤细胞的水平会升高,因为它们会降解 α-突触核蛋白聚集体、破坏衰老神经元并减轻中枢神经系统白细胞引起的神经炎症。
NK 细胞的适应性特征——“记忆样”、 “适应性” 和记忆性 NK 细胞
在原发性感染后产生记忆细胞的能力以及随之而来的对相同抗原的后续感染的快速免疫激活和反应是 T 细胞和 B 细胞在适应性免疫反应中发挥作用的基础。多年来,NK 细胞一直被认为是先天免疫系统的一部分。然而,最近越来越多的证据表明,NK 细胞可以表现出通常归因于适应性免疫细胞(例如 T 细胞反应)的几种特征,例如亚群的动态扩张和收缩、寿命增加和一种免疫记忆形式,其特征是在用相同抗原进行二次攻击时产生更有效的反应。在小鼠中,大多数研究是使用鼠巨细胞病毒 (MCMV) 和半抗原超敏反应模型进行的。特别是在 MCMV 模型中,发现了 MCMV 诱导的 NK 细胞的保护性记忆功能,并且证明了受体 Ly49 对 MCMV 配体 m157 的直接识别对于产生适应性 NK 细胞反应至关重要。在人类中,大多数研究集中在携带激活受体NKG2C ( KLRC2 ) 的 NK 细胞亚群的扩增。此类扩增主要在对人类巨细胞病毒(HCMV)的反应中观察到,但在其他感染中也有观察到,包括汉坦病毒、基孔肯雅病毒、艾滋病毒或病毒性肝炎。然而,这些病毒感染是否会触发适应性 NKG2C+ NK 细胞的扩增,或其他感染是否会导致潜伏性 HCMV 重新激活(如对肝炎的建议 ),仍是一个研究领域。值得注意的是,最近的研究表明,适应性 NK 细胞可以利用激活受体NKG2C ( KLRC2 ) 直接结合人类巨细胞病毒衍生的肽抗原,并通过活化、扩增和分化来响应肽识别,一种应对病毒感染的机制,此前仅见于适应性免疫系统的T 细胞。
妊娠期 NK 细胞功能
由于大多数怀孕涉及的父母双方组织不匹配,因此成功怀孕需要抑制母亲的免疫系统。NK 细胞被认为是此过程中的重要细胞类型。这些细胞被称为“子宫 NK 细胞”(uNK 细胞),它们与外周 NK 细胞不同。它们属于CD56亮NK 细胞亚群,在细胞因子分泌方面具有强大的能力,但细胞毒性能力较低,与外周 CD56亮NK 细胞相对相似,但受体特征略有不同。这些 uNK 细胞是妊娠早期子宫内最丰富的白细胞,约占此处白细胞的 70%,但它们的来源仍存在争议。
这些 NK 细胞有能力在体外引发细胞毒性,但水平低于外周 NK 细胞,尽管含有穿孔素。体内缺乏细胞毒性可能是由于其抑制性受体的配体存在。滋养层细胞下调HLA-A和HLA-B以防御细胞毒性 T 细胞介导的死亡。这通常会通过缺乏自我识别来触发 NK 细胞;然而,这些细胞存活了下来。滋养层细胞选择性保留HLA-E (NK 细胞抑制性受体NKG2A的配体)和HLA-G (NK 细胞抑制性受体KIR2DL4的配体),被认为可以抵御 NK 细胞介导的死亡。
与对照组相比,复发性流产女性的子宫 NK 细胞没有显著差异。然而,复发性流产女性的外周 NK 细胞百分比高于对照组。
NK 细胞分泌大量细胞因子,帮助介导其功能。NK 细胞与HLA-C相互作用,产生滋养层增殖所必需的细胞因子。它们分泌的一些重要细胞因子包括TNF-α、IL-10、IFN-γ、GM-CSF和TGF-β等。例如,IFN-γ 可扩张和变薄母体螺旋动脉壁,以增强流向植入部位的血流。
肿瘤细胞逃避NK细胞攻击
通过脱落诱饵NKG2D可溶性配体,肿瘤细胞可以逃避免疫反应。这些可溶性 NKG2D 配体与 NK 细胞 NKG2D 受体结合,激活假 NK 反应,从而产生对受体位点的竞争。这种逃避方法发生在前列腺癌中。此外,前列腺癌肿瘤能够下调 MHC 1 类分子的表达,从而逃避 CD8 细胞识别。这种免疫逃避的例子实际上凸显了 NK 细胞在肿瘤监视和反应中的重要性,因为 CD8 细胞只能在 NK 启动的细胞因子产生(适应性免疫反应)后才对肿瘤细胞起作用。
NK 细胞过多
NK 细胞的实验性治疗导致细胞因子过度产生,甚至引起感染性休克。炎症细胞因子干扰素γ的消耗可逆转这种影响。[需要引证]
应用
抗癌治疗
据报道,肿瘤浸润 NK 细胞在促进人类三阴性乳腺癌中药物诱导的细胞死亡方面起着关键作用。由于 NK 细胞在表达非自身 HLA 抗原(但不识别自身)时会识别靶细胞,因此自体(患者自身的)NK 细胞输注未显示出任何抗肿瘤作用。相反,研究人员正在研究使用来自外周血的同种异体细胞,这需要在输注到患者体内之前去除所有 T 细胞,以消除可能致命的移植物抗宿主病的风险。这可以通过使用免疫磁性柱 (CliniMACS) 来实现。此外,由于血液中的 NK 细胞数量有限(只有 10% 的淋巴细胞是 NK 细胞),因此需要在培养中扩增它们的数量。这可能需要几周时间,且产量取决于供体。
CAR-NK 细胞
嵌合抗原受体(CAR) 是针对细胞表面抗原的基因改造受体,它为增强效应细胞功效提供了一种有价值的方法。CAR 诱导携带这些受体的效应细胞与表达靶抗原的细胞高亲和力结合,从而降低细胞激活的阈值并诱导效应功能。
CAR-T 细胞现在是一种相当知名的细胞疗法。然而,其更广泛的应用受到几个基本问题的限制:CAR-T 细胞疗法成本高,这是因为需要为每位患者生成特定的 CAR-T 细胞;必须仅使用自体 T 细胞,因为如果使用同种异体 T 细胞,则存在GvHD的高风险;如果患者复发或观察到 CAR-T 细胞存活率低,则无法重新输注 CAR-T 细胞;CAR-T 疗法还具有高毒性,主要是由于IFN-γ 的产生以及随后诱导的 CRS(细胞因子释放综合征)和/或神经毒性。
CAR NK 细胞的使用不受需要生成患者特异性细胞的限制,同时,GvHD 不是由 NK 细胞引起的,因此无需自体细胞。使用 CAR NK 细胞时,未观察到 CAR T 疗法的毒性作用,例如 CSR。因此,NK 细胞被认为是一种有趣的“现成”产品选择。与 CAR T 细胞相比,CAR NK 细胞保持 NK 细胞活化受体的表达不变。因此,即使由于肿瘤细胞的肿瘤逃逸策略,CAR 受体的配体表达下调,NK 细胞也能识别并杀死肿瘤细胞。
脐带血来源的 NK 细胞已被用于生成 CAR.CD19 NK 细胞。这些细胞能够自我产生细胞因子IL-15,从而增强自分泌/旁分泌表达和体内持久性。这些改良的 NK 细胞的给药与 CSR、神经毒性或 GvHD 的发展无关。
FT596 产品是首个获准在美国用于临床研究的、源自iPSC的“现成”、通用且同种异体的 CAR NK 细胞产品。它由针对 NK 细胞优化的抗 CD19 CAR 组成,具有针对NKG2D激活受体的跨膜结构域、2B4 共刺激结构域和 CD3ζ 信号结构域。添加了两个额外的关键组件:1) 高亲和力、不可裂解的 Fc 受体 CD16 (hnCD16),可实现肿瘤靶向和增强抗体依赖性细胞毒性,而不会产生负调节,结合 2) 靶向肿瘤细胞的治疗性单克隆抗体和促进细胞因子非依赖性持久性的 IL-15/IL-15 受体融合蛋白 (IL-15RF)。
NK-92细胞
获得大量 NK 细胞的更有效方法是扩增NK-92 细胞,这是一种 NK 细胞系,具有高活性血液自然杀伤 (NK) 细胞的所有特征,但具有更广泛和更高的细胞毒性。NK-92 细胞在培养中不断生长,可以在袋子或生物反应器中扩增到临床级数量。临床研究表明,NK-92 细胞是安全的,并且在患有肺癌或胰腺癌、黑色素瘤和淋巴瘤的患者中表现出抗肿瘤活性。当 NK-92 细胞源自淋巴瘤患者时,必须在输注前进行辐照。然而,人们正在努力对细胞进行工程改造,以消除对辐照的需要。辐照过的细胞保持完全的细胞毒性。NK-92 是同种异体(来自不同于接受者的供体),但临床研究表明不会引起显著的宿主反应。
未经改造的 NK-92 细胞缺乏 CD-16,因此无法发挥抗体依赖性细胞毒作用 (ADCC);然而,这些细胞经过改造后可表达高亲和力 Fc 受体 (CD16A, 158V),该受体与 IL-2 基因相关,可与内质网 (ER) 结合。这些高亲和力 NK-92 细胞可发挥 ADCC 作用,大大扩展了治疗效用。
NK-92 细胞也经过改造,可表达嵌合抗原受体 (CAR),其方法与 T 细胞类似。例如,NK-92 衍生细胞经过改造,可表达 CD16 和抗 PD-L1 CAR;目前正在进行肿瘤适应症的临床开发。已生成表达 HER2 (ErbB2) CAR 的临床级 NK-92 变体,目前正在对 HER2 阳性胶质母细胞瘤患者进行临床研究。已生成其他几个表达 PD-L1、CD19、HER-2 和 EGFR CAR 的临床级克隆。在正在进行的 I/II 期研究中,已将 PD-L1 靶向的高亲和力 NK 细胞用于许多实体瘤患者。
NKG2D-Fc融合蛋白
在波士顿儿童医院与丹娜法伯癌症研究所合作开展的一项研究中,免疫功能低下的小鼠因EBV感染而患上淋巴瘤,一种名为NKG2D的 NK 激活受体与 EBV 抗体的刺激性Fc部分融合。NKG2D-Fc 融合被证明能够减缓肿瘤生长并延长接受者的生存期。在 LMP1 引发的淋巴瘤移植模型中,NKG2D-Fc 融合被证明能够减缓肿瘤生长并延长接受者的生存期。
在霍奇金淋巴瘤中,恶性霍奇金 Reed-Sternberg 细胞通常缺乏 HLA I 类,免疫逃避部分是由向耗竭的 PD-1hi NK 细胞表型倾斜所介导的,而这些 NK 细胞的重新激活似乎是检查点阻断诱导的一种作用机制。
TLR 配体
通过TLR信号传导可在体内和体外有效激活 NK 细胞效应功能。TLR 配体随后有可能在 NK 细胞抗肿瘤免疫治疗期间增强 NK 细胞效应功能。
曲妥珠单抗是一种单克隆抗 HER2抗体,用于治疗HER2+ 乳腺癌。NK 细胞是曲妥珠单抗治疗效果的重要组成部分,因为 NK 细胞可以识别抗体包被的癌细胞,从而诱导ADCC(抗体依赖性细胞毒性)反应。除曲妥珠单抗外,还使用 TLR 配体作为增强其效果的手段。从云芝中提取的多糖云芝是TLR-2的有效配体,因此可激活 NK 细胞,诱导IFNg的产生并增强曲妥珠单抗包被细胞识别引起的ADCC 。
TLR-7的刺激会诱导IFN 类型 I和其他促炎细胞因子(如IL-1b、IL-6和IL-12)的表达。患有NK 细胞敏感性淋巴瘤 RMA-S 的小鼠接受了 SC1 分子治疗。SC1 是一种新型小分子 TLR-7 激动剂,据报道,重复给药会以 TLR-7 和 IFN 类型 I 依赖的方式激活 NK 细胞,从而逆转 NK 细胞无能状态,最终导致肿瘤溶解。
VTX-2337是一种选择性TLR-8激动剂,与单克隆抗体 西妥昔单抗一起用作治疗复发性或转移性SCCHN的潜在疗法。结果表明,在使用 VTX-2337 进行预处理后,NK 细胞对西妥昔单抗抗体的治疗反应性更强。这表明 TLR-8 的刺激和随后炎症小体的激活增强了接受西妥昔单抗抗体治疗的患者的CD-16介导的ADCC反应。
NK 细胞在控制HIV-1感染中发挥作用。TLR 是先天抗病毒免疫的强效增强剂,并可能逆转 HIV-1 潜伏期。外周血单核细胞与新型强效TLR-9配体MGN1703孵育可增强 NK 细胞效应功能,从而显著抑制自体 CD4+ T 细胞培养中 HIV-1 的扩散。NK 细胞中 TLR-9 的刺激可诱导强大的抗病毒先天免疫反应,增加 HIV-1转录(表明病毒潜伏期逆转),并且还增强了 NK 细胞介导的自体 CD4+ T 细胞中 HIV-1 感染的抑制。
新发现
对艾滋病毒的先天抵抗力
最近的研究表明,特定的 KIR-MHC I 类基因相互作用可能控制着对某些病毒感染(包括HIV及其随后的艾滋病)的先天遗传抵抗力。研究发现,某些 HLA 同种型可决定 HIV 向艾滋病的进展;例如,HLA-B57和HLA-B27等位基因可延缓 HIV 向艾滋病的进展。这一点显而易见,因为表达这些 HLA 等位基因的患者的病毒载量较低,CD4 + T细胞数量下降较为缓慢。尽管进行了大量研究并收集了大量数据来衡量 HLA 等位基因和 KIR 同种型的遗传相关性,但尚未得出哪种组合可降低 HIV 和艾滋病易感性的确切结论。
NK 细胞可以对 HIV 施加免疫压力,此前有报道称这种压力仅存在于 T 细胞和抗体中。 HIV 会变异以逃避 NK 细胞的检测。
组织驻留 NK 细胞
我们目前的大部分知识都来自对小鼠脾脏和人类外周血 NK 细胞的研究。然而,近年来,组织驻留 NK 细胞群已被描述。这些组织驻留 NK 细胞与之前描述的组织驻留记忆 T 细胞具有转录相似性。然而,组织驻留 NK 细胞不一定具有记忆表型,事实上,大多数组织驻留 NK 细胞在功能上尚未成熟。这些特殊的 NK 细胞亚群可以在器官稳态中发挥作用。例如,NK 细胞在具有特定表型的人类肝脏中富集,并参与控制肝纤维化。组织驻留 NK 细胞也在骨髓、脾脏等部位被发现,最近在肺、肠和淋巴结中也被发现。在这些部位,组织驻留 NK 细胞可能充当人类一生中维持未成熟 NK 细胞的储存器。
针对白血病靶点的适应性NK细胞
自然杀伤细胞正在被研究作为一种治疗急性髓系白血病 (AML) 患者的新兴疗法,而细胞因子诱导的记忆样 NK 细胞已显示出增强的抗白血病功能的前景。研究显示,这种 NK 细胞可增强干扰素-γ 的产生和对患者白血病细胞系和原发性 AML 母细胞的细胞毒性。在 1 期临床试验中,9 名患者中有 5 名对治疗表现出临床反应,4 名患者完全缓解,这表明这些 NK 细胞在未来作为 AML 患者成功的转化免疫治疗方法具有巨大潜力。
热门产品推荐
-

HELA人宫颈癌细胞(STR鉴定正确)
¥1200元
-
HSF人皮肤成纤维细胞(免疫荧光鉴定)
¥1800元
-

HepG2人肝癌细胞(STR鉴定正确)
¥1200元
-

A549人非小细胞肺癌细胞(STR鉴定正确)
¥1200元
-
H9C2大鼠心肌细胞
¥1200元
-

4T1小鼠乳腺癌细胞(STR鉴定正确)
¥1200元
大家都在看
-
人源肿瘤细胞系异体移植(cell derived xenograft, CDX),即将体外传代培养的肿瘤细胞接种至免疫缺陷小鼠,因其有明确的肿瘤生长动力学、易于遗传操作、成瘤率高、价格低廉等特点,并且能够产生一致和可重复的数据,···...
阅读详情 -
hiPSC人诱导多能干细胞培养教程:在培养hiPSC细胞前,需准备好hESC/iPSC完全培养基配制和Matrigel铺板,hiPSC人诱导多能干细胞复苏操作,1. 将水浴锅预热至37℃;并将Matrigel包被的6孔板,提前放置生物安全柜中约1小时恢复···...
阅读详情 -
H9人胚胎干细胞培养条件与方法:1. 将水浴锅预热至37℃,并将Matrigel包被的6孔板,提前放置生物安全柜中约1小时恢复至室温(15~30℃);2. 取4 mL hESC/iPSC完全培养基,按照1:4000比例加入1 μL的hESC/iPSC Supplement C,···...
阅读详情 -
H1人胚胎干细胞培养指南:在培养h1干细胞之前,首先要准备好hESC/iPSC完全培养基配制, 铺板,H1人胚胎干细胞复苏步骤:1.将水浴锅预热至37℃;并将Matrigel包被的6孔板,提前放置生物安全柜中约1小时恢复至室温(15~30℃);···...
阅读详情 -
4T1细胞培养方法:小鼠乳腺癌4T1细胞培养基 90%DMEM+10% FBS+PS,生长条件:气相:95%空气+5%二氧化碳;温度:37℃,4T1细胞形态特征为上皮细胞样,贴壁生长,如果4T1细胞密度达80%-90%,即可进行传代培养,传代方法:1:2至1:3···...
阅读详情 -
常用人肝癌细胞系有哪些及如何选择:目前较为常用的几株人肝癌细胞系SMMC-7721、Bel-7402、MHCC97、HepG2、Hep3B、Huh-7 and PLC/PRF/5,那么人肝癌细胞株如何选择呢?一方面你可以查找相关的文献,另一方面可以考虑选择···...
阅读详情







